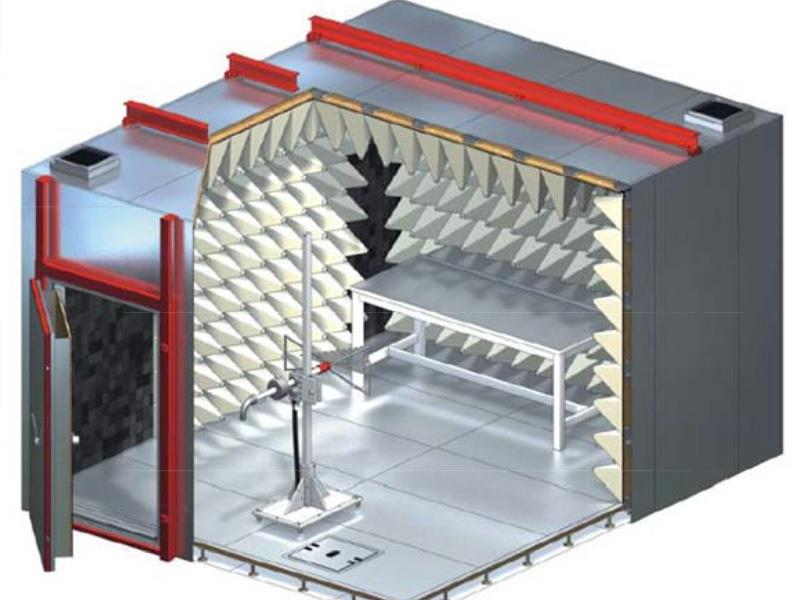
实验室废弃物的处理(实验室静电防护的常用措施)
一般来说不产生静电是不可能的,但有时仅仅产生静电还不足以构成危害,真正的危险往往在于静电的积聚以及由此带来的静电放电,因此防静电的关键是如何使那些已经存在静电荷的地方保持在一定的安全电压以下。电子仪器生产过程中常常采用接地、静电泄露、耗散、中和、增湿,屏蔽等措施达到尽量防止和抑制静电的产生和静电积聚,或是使得已产生的静电积聚迅速、安全、有效地消除的目的,从而对静电破坏进行防护。
温湿度控制
保持一定湿度、温度从表的数据中可以看到,环境湿度对人体活动产生的静电电压影响非常大,静电防护区的相对环境湿度应控制在40%以上。在工艺条件许可时,可以安装空调加湿、喷雾器等以提高空气的相对湿度。
另外,绝对湿度一定时,温度较高的区域会比温度低的区域相对湿度小,因此保持较低的温度对静电防护也是有利的。
良好的接地系统
防静电接地系统是接地泄漏的入地通道,是将接地的地面,墙面,工作台,设备,仪器,腕带等按工作区域使接地电荷顺次入地的电气联结系统。
为了有效防止静电产生危害,必需给静电防护环境中的所有导体(包括人员)提供一条信道,使静电在较短时间内(如O.1S)及时、安全地泄放,即通常所说的静电接地。可靠的接地提供“等电位”效果,可以有效减少静电对静电敏感器件造成的伤害。
总之,一切与器件相接触的物体,包括空间都应有防静电措施,构成一个完整的静电防护区域,基本的静电防护工作区接地情况参见下图
该系统必须要有独立的,可靠的接地装置接地电阻应小于10ohm(防静电地线不得接在电源零线上,不得与防雷地线共用,如使用三相五线制供电,其大地线可作为防静电地线,但零线、地线不得混接)接地主干线截面积应小于100mm2,支干线截面积应小于6mm2,设备和工作台的接地线应采用截面积应不小于1.25mm2的多股敷塑导线 接地线颜色以黄绿色线为宜 接地主干线的连接方式应采用钎焊。实验室专用地线埋设如图所示。专用地线应埋在建筑物的阴面潮湿处地线可由一块长600~700mm宽400~500mm厚4~5mm的紫铜板及钎焊在紫铜板上的引出线;截面积不小于100mm2的扁铜线<组成
废弃物,包含的种类繁多。从实验室排出的废弃物,主要为列于附录中的物质。排放这些废弃物时,受到政府颁布的各项法令的限制。特别是化学物质,由于考虑到它会以某种形式危及人们的健康,所以从防止污染环境的立场出发,即使数量甚微,也要避免把它排放到自然水域或大气中去,而必须加以适当的处理。
通常从实验室排出的废液,虽然与工业废液相比在数量上是很少的,但是,由于其种类多,加上组成经常变化,因而最好不要把它集中处理,而由各个实验室根据废弃物的性质,分别加以处理。为此,废液的回收及处理自然就需依赖实验室中每一个工作人员。所以,实验人员应予足够的重视,疏忽大意固然不对,而即使由于操作错误或发生事故,也应避免排出有害物质。同时,实验人员还必须加深对防止公害的认识,自觉采取措施,防止污染,以免危害自身或者危及他人。
收集、贮存一般应注意的事项
1).废液的浓度超过表4—1所列的浓度时,必须进行处理。但处理设施比较齐全时,往往把废液的处理浓度限制放宽。
2).最好先将废液分别处理,如果是贮存后一并处理时,虽然其处理方法将有所不同,但原则上仍如表4—1所列的方法,将可以统一处理的各种化合物收集后进行处理。
3).处理含有络离子、螯合物之类的废液时,如果有干扰成份存在,要把含有这些成份的废液另外收集。
4).下面所列的废液不能互相混合:
①过氧化物与有机物;②氰化物、硫化物、次氯酸盐与酸;③盐酸、氢氟酸等挥发性酸与不挥发性酸;④浓硫酸、磺酸、羟基酸、聚磷酸等酸类与其它的酸;⑤铵盐、挥发性胺与碱。
5).要选择没有破损及不会被废液腐蚀的容器进行收集。将所收集的废液的成份及含量,贴上明显的标签,并置于安全的地点保存。特别是毒性大的废液,尤要十分注意。
6).对硫醇、胺等会发出臭味的废液和会发生氰、磷化氢等有毒气体的废液,以及易燃性大的二硫化碳、乙醚之类废液,要把它加以适当的处理,防止泄漏,并应尽快进行处理。
7).含有过氧化物、硝化甘油之类爆炸性物质的废液,要谨慎地操作,并应尽快处理。
8).含有放射性物质的废弃物,用另外的方法收集,并必须严格按照有关的规定,严防泄漏,谨慎地进行处理。
表4—1 必须加以处理的废液的最低浓度、收集分类及处理方法
【注】①上表所列的浓度为金属或所标明的化合物的浓度。
②虽然是有机类废液,但也含有列于无机类废液的物质,如果无机物质的浓度超过列于无机类该项浓度时,该废液应另行收集。
③有机类废液的浓度系指含水废液的浓度。
处理时一般应注意的事项
1).随着废液的组成不同,在处理过程中,往往伴随着产生有毒气体以及发热、爆炸等危险。因此,处理前必须充分了解废液的性质,然后分别加入少量所需添加的药品。同时,必须边注意观察边进行操作。
2).含有络离子、螯合物之类物质的废液,只加入一种消除药品有时不能把它处理完全。因此,要采取适当的措施,注意防止一部份还未处理的有害物质直接排放出去。
3).对于为了分解氰基而加入次氯酸钠,以致产生游离氯,以及由于用硫化物沉淀法处理废液而生成水溶性的硫化物等情况,其处理后的废水往往有害。因此,必须把它们加以再处理。
4).沾附有有害物质的滤纸、包药纸、棉纸、废活性炭及塑料容器等东西,不要丢入垃圾箱内。要分类收集,加以焚烧或其它适当的处理,然后保管好残渣。
5).处理废液时,为了节约处理所用的药品,可将废铬酸混合液用于分解有机物,以及将废酸、废碱互相中和。要积极考虑废液的利用。
6).尽量利用无害或易于处理的代用品(参照附录表6),代替铬酸混合液之类会排出有害废液的药品。
7).对甲醇、乙醇、丙酮及苯之类用量较大的溶剂,原则上要把它回收利用,而将其残渣加以处理。
无机类实验废液的处理方法
1.含六价铬的废液
注意事项
1).要戴防护眼镜、橡皮手套,在通风橱内进行操作。
2).把Cr(Ⅵ)还原成Cr(Ⅲ)后,也可以将其与其它的重金属废液一起处理。
3).铬酸混合液系强酸性物质,故要把它稀释到约1%的浓度之后才进行还原。并且,待全部溶液被还原变成绿色时,查明确实不含六价铬后,才按操作步骤中从第四点开始进行处理。
处理方法[还原、中和法(亚硫酸氢钠法)]
[原理]
Cr(Ⅵ)不管在酸性还是碱性条件下,总以稳定的铬酸根离子状态存在。因此,可按照下式将Cr(Ⅵ)还原成Cr(Ⅲ)后进行中和,使之生成难溶性的Cr(OH)3沉淀而除去。
4H2CrO4+6NaHSO3+3H2SO4→2Cr2(SO4)3+3Na2SO4+10H2O………(1)
Cr2(SO4)3+6NaOH→2Cr(OH)3↓+3Na2SO4………(2)
(1)式还原反应,若pH值在3以下,反应在短时间内即进行结束。如果使(2)式中和反应pH值在7.5~8.5范围内进行,则Cr(Ⅲ)即以Cr(OH)3再溶解。
[操作步骤]
1).于废液中加入H2SO4,充分搅拌,调整溶液pH值在3以下(采用pH试纸或pH计测定。对铬酸混合液之类废液,已是酸性物质,不必调整pH值)。
2).分次少量加入NaHSO3结晶,至溶液由黄色变成绿色为止,要一面搅拌一面加入(如果使用氧化——还原光电计测定,则很方便)。
3).除Cr以外还含有其它金属时,确证Cr(Ⅵ)转化后,作含重金属的废液处理。
4).废液只含Cr重金属时,加入浓度为5%的NaOH溶液,调节pH值至7.5~8.5(注意,pH值过高沉淀会再溶解)。
5).放置一夜,将沉淀滤出并妥善保存(如果滤液为黄色时,要再次进行还原)。
6).对滤液进行全铬检测,确证滤液不含铬后才可排放。
[Cr(Ⅵ)的分析]
定性分析采用二苯基碳酰二肼试纸或检测箱进行检测;定量分析则用二苯基碳酰二肼吸光光度法[详见“日本工业标准规格”(以下简称JIS) K 0102 51.2.1]和原子吸收光谱分析法进行测定。但要注意Cu、Cd、V、Mo、Hg、Fe等离子的干扰。
[全Cr分析]
用高锰酸钾氧化Cr(Ⅲ)使之变成Cr(Ⅵ),然后进行分析。
[备注]
1).除上述处理方法外,还有用强碱性阴离子交换树脂吸附Cr(Ⅵ)的方法。此法即使废液含铬浓度较低也很有效。
2).用作还原Cr(Ⅵ)的还原剂,有表4—2所列的物质。而作为中和剂,也可以用Ca(OH)2。不过,其泥浆沉淀物较多。
表4—2 可用作还原铬化合物的还原剂
2.含氰化物的废液
注意事项
1).因有放出毒性气体的危险,故处理时要慎重。操作时最好在通风橱内进行。
2).废液要制成碱性,不要在酸性情况下直接放置。
3).对难于分解的氰化物(如Zn、Cu、Cd、Ni、Co、Fe等的氰的络合物)以及有机氰化物的废液,必须另行收集处理。
4).对其含有重金属的废液,在分解氰基后,必须进行相应的重金属的处理。
处理方法(氯碱法)
[原理]
用含氮氧化剂将氰基分解为N2和CO2。反应按如下两个阶段进行:
(1)式反应在pH值大于10的条件下进行。若pH值在10以下就加入氧化剂,则会发生如下反应:
而产生刺激性很大的有害气体CNCl,因而处理时必须特别注意。对(2)式反应,如果pH值过高,则反应时间过长,故调整pH在8左右进行较好。
[操作步骤]
1).于废液中加入NaOH溶液,调整pH至10以上。然后加入约10%的NaOCl溶液,搅拌约20分钟,再加入NaOCl溶液,搅拌后,放置数小时(如果用氧化——还原光电计检测其反应终点,则较方便)。
2).加入5—10%的H2SO4(或盐酸),调节 pH至7.5~8.5,然后放置一昼夜。
3).加入Na2SO3溶液,还原剩余的氯(稍微过量时,可用空气氧化。每升含1克Na2SO3的溶液1毫升,相当于0.55毫克Cl)。
4).查明废液确实没有CN-离子后,才可排放。
5).废液含有重金属时,再将其作含重金属的废液加以处理。
[分析方法]
定性分析采用氰离子试纸或检测箱进行检测;定量分析则蒸出全部氰后(见JIS K 0102 29.1.2),用硫氰酸汞法(见JIS K 0102 29.3)进行分析。
[备注]
1).除上述处理方法外,还有以下几种方法:电解氧化法(对含氰化物2克/升以上的高浓度废液较为有效,而处理含有Co、Ni、Fe络合物的废液,则较困难);普鲁士蓝法(是以生成铁氰化合物的形式使之沉淀的方法,此法处理含有大量重金属的废液,较为有利。但要彻底处理,则较为困难);以及臭氧氧化法(用Cu、Mn离子加快反应,在pH为11~12下进行反应,即可把废液转变为无害)。
2).其它可用作氰化物氧化剂的,有表4—3所列的物质。
3).对Fe、Ni、Co等的含氰络合物,用上述方法难以分解。因而必须采用下述方法进行处理:
①于废液中加入NaOH溶液,调整 pH至 10以上,接着加入NaOCl溶液,加热2小时左右,冷却后过滤沉淀。
②在废液中加入H2SO4,调整pH至3以下,加热约2小时,冷却后过滤沉淀。
③用阴离子交换树脂吸附。
4).对有机氰化物,分别施行上述无机类废液的处理后,作为有机类废液处理。对难溶于水的有机氰化物,用氢氧化钾酒精溶液使之转变成氰酸盐,然后才进行处理。
表4—3 能作氧化氰化物的氧化剂
【注】:如果有Cu+、Ni+等离子存在,必须加入过量的氧化剂。
3.含镉及铅的废液
注意事项
1).含重金属两种以上时,由于其处理的最适宜pH值各不相同,因而,对处理后的废液必须加以注意。
2).含大量有机物或氰化物的废液,以及含有络离子的时候,必须预先把它分解除去(参照含有重金属的有机类废液的处理方法)。
镉的处理方法(氢氧化物沉淀法)
[原理]
用Ca(OH)2将Cd2+转化成难溶于水的Cd(OH)2而分离。
Cd2++Ca(OH)2→Cd(OH)2↓+Ca2+
当pH值在11附近时,Cd(OH)2的溶解度最小,因此调节pH值很重要。但是,若有金属离子共沉淀时,那么,即使pH值较低也会产生沉淀。
[操作步骤]
1).在废液中加入 Ca(OH)2,调节pH至10.6~11.2,充分搅拌后即放置。
2).先过滤上层澄清液,然后才过滤沉淀。保管好沉淀物。
3).检查滤液中确实不存在Cd2+离子时,把它中和后即可排放。
[分析方法]
定性分析用镉试剂试纸法或检测箱进行检测;定量分析则用二苯基硫巴腙(即双硫腙)吸光光度法(见JIS K 0102 40.1)或原子吸收光谱分析法进行测定。
铅的处理方法(氢氧化物共沉淀法)
[原理]
用Ca(OH)2把Pb2+转变成难溶性的Pb(OH)2,然后使其与凝聚剂共沉淀而分离。
Pb2++Ca(OH)2→Pb(OH)2↓+Ca2+
为此,首先把废液的pH值调整到11以上,使之生成Pb(OH)2。然后加入凝聚剂,继而将pH值降到7~8,即产生Pb(OH)2共沉淀。但如果pH值在11以上,则生成HPbO2-而沉淀会再溶解。
[操作步骤]
1).在废液中加入Ca(OH)2,调整pH值至11。
2).加入Al2(SO4)3(凝聚剂),用H2SO4慢慢调节pH值,使其降到7~8。
3).把溶液放置,待其充分澄清后即过滤。检查滤液不含Pb2+后,即可排放。
[分析方法]
定性分析用检测箱进行(注意干扰离子)。定量分析用二苯基硫巴腙(即双硫腙)吸光光度法(见JIS K 0102 39.1)或原子吸收光谱分析法。
[备注]
1).除上述处理方法外,还有硫化物沉淀法(其生成的硫化物溶解度较小,但因形成胶体微粒而难于分离);碳酸盐沉淀法(生成的沉淀微粒细小,分离困难);吸附法(使用强酸性阳离子交换树脂,几乎能把它们完全除去)。
2).碱性药剂也可以用NaOH,但是由于生成微粒状沉淀而难于过滤,故用Ca(OH)2较好。
4. 含砷废液
注意事项
1).As2O3是剧毒物质,其致命剂量为0.1克。因此,处理时必须十分谨慎。
2).含有机砷化合物时,先将其氧化分解,然后才进行处理(参照含重金属有机类废液的处理方法)。
处理方法(氢氧化物共沉淀法)
[原理]
用中和法处理不能把 As沉淀。通常使它与Ca、Mg、Ba、Fe、Al等的氢氧化物共沉淀而分离除去。用Fe(OH)3时,其最适宜的操作条件是:铁砷比(Fe/As)为30~50;pH为7~10。
[操作步骤]
1).废液中含砷量大时,加入Ca(OH)2溶液,调节pH至9.5附近,充分搅拌,先沉淀分离一部份砷。
2).在上述滤液中,加入FeCl3,使其铁砷比达到50,然后用碱调整pH至7~10之间,并进行搅拌。
3).把上述溶液放置一夜,然后过滤,保管好沉淀物。检查滤液不含As后,加以中和即可排放。此法可使砷的浓度降到0.05ppm以下。
[分析方法]
定量分析有铁共沉淀、浓缩——溶剂萃取——钼蓝法(见JIS K 0102 48.1);或铁共沉淀、浓缩——分离砷化氢——二乙基氨荒酸银法进行测定(见JIS K 0102 48.2)。
[备注]
除上述处理方法外,还有硫化物沉淀法(用盐酸酸化,然后用H2S或NaHS等试剂使之沉淀)及吸附法(用活性炭、活性矾土作吸附剂)。
5. 含汞废液
注意事项
1).废液毒性大,经微生物等的作用后,会变成毒性更大的有机汞。因此,处理时必须做到充分安全。
2).含烷基汞之类的有机汞废液,要先把它分解转变为无机汞,然后才进行处理(参照有机汞的处理方法)。
3).不能含有金属汞。
处理方法之一(硫化物共沉淀法)
[原理]
用Na2S或NaHS把Hg2+转变为难溶于水的HgS,然后使其与Fe(OH)3共沉淀而分离除去。如果使其pH值在10以上进行反应,HgS即变成胶体状态。此时,即使用滤纸过滤,也难于把它彻底清除。如果添加的Na2S过量时,则生成[HgS2]2-而沉淀容易发生溶解。腘a2S过量时,则生成[HgS2]2-而沉淀容易发生溶解。
[操作步骤]
1).于废液中加入对于FeSO4(10ppm)及Hg2+之浓度的1∶1当量的Na2S·9H2O,充分搅拌,并使废液之pH值保持在6~8范围内。
2).上述溶液经放置后,过滤沉淀并妥善保管好滤渣(用此法处理,可使Hg浓度降到0.05ppm以下)。
3).再用活性炭吸附法或离子交换树脂等方法,进一步处理滤液。
4).在处理后的废液中,确证检不出Hg后,才可排放。
处理方法之二(活性炭吸附法)
先稀释废液,使 Hg浓度在1ppm以下。然后加入NaCl,再调整pH值至6附近,加入过量的活性炭,搅拌约2小时,然后过滤,保管好滤渣。此法也可以直接除去有机汞。
处理方法之三(离子交换树脂法)
于含汞废液中加入NaCl,使之生成[HgCl4]2-络离子而被阴离子交换树脂所吸附。但随着汞的形态不同,有时此法效果不够理想。并且,当有有机溶剂存在时,此法也不适用。
[分析方法]
全汞的定量分析,用高锰酸钾分解——二苯基硫巴腙吸光光度法(见JIS K 0102 44.1.1)或用原子吸收光谱分析法。定性分析虽然也可以用检测箱进行,但若从其检出限度考虑,用它不能检测达到排放标准那样低浓度的废液。
[备注]
1).因为汞容易形成络离子,故处理时必须考虑汞的存在形态。
2).若用NaHS和ZnCl2代替Na2S+FeSO4,可以把汞清除到极微量的程度。例如,对含Hg 10ppm的废液1升,pH值在10.3,加入32毫克NaHS及80毫克ZnCl2进行处理。处理后,Hg的浓度降至0.003ppm。
6. 含有机汞的废液
注意事项
含烷基汞之类废液,毒性特别大,处理时必须十分注意。
处理方法(氧化分解法)
用下述处理方法,先将有机汞转变成无机汞,然后再进行处理。
[操作步骤]
在500毫升废液(含汞0.025毫克以下)中,加入浓硝酸60毫升及 6%的KMnO4水溶液20毫升,加热回流二小时。待KMnO4溶液的颜色消失时,把温度降到60℃以下,然后加入2毫升KMnO4溶液,再加热溶液。
[分析方法]
以烷基汞为对象的定量分析方法有:气相色谱法(见JISK 0102 44.2.1)和薄层色谱分离——二苯基硫巴腙吸光光度法(见JIS K 0102 44.2.2)。全汞的定量分析方法,与上述JIS K 0102 44.1.1所述方法相同。
[备注]
除上述的处理方法外,还有用NaOCl和NaOH或KMnO4和H2SO4进行氧化,以及用活性炭吸附等方法。
7. 含重金属的废液
注意事项
1).对含有机物、络离子及螯合物量大的废液,要先把它们分解除去(参照含重金属的有机类废液的处理方法)。
2).含Cr(Ⅲ)、CN等物质时,也要预先进行上述处理。
3).废液中含有两种以上的重金属时,因其处理的最适宜的pH值各不相同,必须加以注意。
处理方法
[原理]
把重金属离子转变成难溶于水的氢氧化物或硫化物等的盐类,然后进行共沉淀而除去。
1).氢氧化物共沉淀法
[操作步骤]
①在废液中加入FeCl3或Fe2(SO4)3,并加以充分搅拌。
②将Ca(OH)2制成石灰乳,然后加入上述废液中,调整 pH至 9~11(如果pH值过高,沉淀会再溶解)。
③溶液经放置后,过滤沉淀物。检查滤液确实不含重金属离子后,才把它中和排放。
[备注]
①如果含有螯合物时,往往不产生沉淀。但是,本法可以除去少量的螯合物。
②按照本法处理,可使Ca、Zn、Fe、Mn、Ni、Cr(Ⅲ)、As、Sb、Al、Co、Ag、Sn、Bi、及其它很多重金属生成氢氧化物沉淀而除去。
③共沉剂也可以用Al2(SO4)3或ZnCl2等物质。
④因在强碱性下,两性金属的沉淀会发生溶解。故要注意其最适宜的pH值(两性金属沉淀溶解的pH值为:Al3+:8.5;Cr3+:9.2;Sn2+:10.6;Zn2+:>11;Pb2+:>11。但是,用共沉淀法处理时,由于产生沉淀的 pH值范围相当宽,因而,在pH值为9~11的条件下,全都能完全沉淀)。
⑤中和剂与其用HaOH,不如用Ca(OH)2为好。因Ca(OH)2可防止两性金属的沉淀再溶解,且其沉降性能也较好。
⑥如果用碳酸钠作中和剂,还可使Ca2+、Sr2+、Ba2+等离子生成难溶性的碳酸盐而除去(pH=10~11)。
2).硫化物共沉淀法
[操作步骤]
①废液中重金属的浓度要用水稀释至1%以下。
②加入Na2S或NaHS溶液,并充分搅拌。
③加入NaOH溶液,调整pH值至9.0~9.5。
④加入FeCl3溶液,调节pH值至8.0以上,然后放置一夜。
⑤用倾析法过滤沉淀,检查滤液确实不含重金属。
⑥再检查滤液有无S2-离子。如果含有S2-离子时,用H2O2将其氧化,中和后即可排放。
[分析方法]
定性分析用检测箱进行,或用二苯基硫巴腙(即双硫腙)溶液,检查有无产生颜色。定量分析则用二苯基硫巴腙吸光光度法或原子吸收光谱分析法(见JIS K 0102)。
[备注]
除上述的处理方法外,还有碳酸盐法(可用含碳酸钠的碱灰浆)、离子交换树脂法及吸附法(用活性炭)等。
8. 含重金属的有机类废液
处理方法
先将妨碍处理重金属的有机物质,用氧化、吸附等适当的处理方法把它除去。然后才把它作无机类废液处理。
1).焚烧法
将含大量有机溶剂废液及有机物的溶液,进行焚烧处理,保管好残渣。
2).氧化分解法
参照含有机汞废液的处理方法。
3).活性炭吸附法
调整pH值至5左右,加入活性炭粉末,经常加以搅拌,经2~3小时后进行过滤(此法适用于处理稀溶液)。
9. 含钡废液
处理方法
在废液中加入Na2SO4溶液,过滤生成的沉淀后,即可排放。
10. 含硼废液
处理方法
把废液浓缩,或者用阴离子交换树脂吸附。对含有重金属的废液,按含重金属废液的处理方法进行处理。
11. 含氟废液
处理方法
于废液中加入消化石灰乳,至废液充分呈碱性为止,并加以充分搅拌,放置一夜后进行过滤。滤液作含碱废液处理。此法不能把氟含量降到8ppm以下。要进一步降低氟的浓度时,需用阴离子交换树脂进行处理。
12. 含氧化剂、还原剂的废液
注意事项
1).原则上将含氧化剂、还原剂的废液分别收集。但当把它们混合没有危险性时,也可以把它们收集在一起。
2).含铬酸盐时可作为含Cr(Ⅵ)的废液处理。
3).含重金属物质时,可作为含重金属的废液处理。
4).不含有害物质而其浓度在1%以下的废液,把它中和后即可排放。
处理方法
[操作步骤]
1).查明各氧化剂和还原剂,如果将其混合也没有危险性时,即可一面搅拌,一面将其中一种废液分次少量加入另一种废液中,使之反应。
2).取出少量反应液,调成酸性,用碘化钾——淀粉试纸进行检验。
3).试纸变蓝时(氧化剂过量):调整pH值至3,加入Na2SO3(用Na2S2O3、FeSO4也可以)溶液,至试纸不变颜色为止。充分搅拌,然后把它放置一夜。
4).试纸不变色时(还原剂过量):调整pH值至3,加入H2O2使试纸刚刚变色为止。然后加入少量Na2SO3,把它放置一夜。
5).不管哪一种情况,都要用碱将其中和至 pH为 7,并使其含盐浓度在5%以下,才可排放。
13. 含酸、碱、盐类物质的废液
注意事项
1).原则上将酸、碱、盐类废液分别收集。但如果没有妨碍,可将其互相中和,或用其处理其它的废液。
2).对含重金属及含氟的废液,要另外收集处理。
3).对黄磷、磷化氢、卤氧化磷、卤化磷、硫化磷等的废液,在碱性情况下,用H2O2将其氧化后,作为磷酸盐废液处理。对缩聚磷酸盐的废液,用硫酸酸化,然后将其煮沸2~3小时进行水解处理。
4).对其稀溶液,用大量水把它稀释到1%以下的浓度后,即可排放。
处理方法
[操作步骤]
1)查明即使将酸、碱废液互相混合也没有危险时,可分次少量将其中一种废液,加入另一种废液中。
2).用pH试纸(或pH计)检验,使加入的酸或碱的废液至溶液的pH约等于7。
3).用水稀释,使溶液浓度降到5%以下,然后把它排放。
14. 含无机卤化物的废液
处理方法
[操作步骤]
1).将含AlBr3、AlCl3、ClSO3H、SnCl4及TiCl4等无机类卤化物的废液,放入大号蒸发皿中,撒上高岭土——碳酸钠(1∶1)的干燥混合物。
2).把它充分混合后,喷洒1∶1的氨水,至没有NH4Cl白烟放出为止。
3).把它中和后放置,过滤沉淀物。检查滤液有无重金属离子。若无,则用大量水稀释后,即可排放。
有机类实验废液的处理方法
注意事项
1).尽量回收溶剂,在对实验没有妨碍的情况下,把它反复使用。
2).为了方便处理,其收集分类往往分为:a)可燃性物质;b)难燃性物质;c)含水废液;d)固体物质等。
3).可溶于水的物质,容易成为水溶液流失。因此,回收时要加以注意。但是,对甲醇、乙醇及醋酸之类溶剂,能被细菌作用而易于分解。故对这类溶剂的稀溶液,经用大量水稀释后,即可排放。
4).含重金属等的废液,将其有机质分解后,作无机类废液进行处理。
处理方法
1).焚烧法
①将可燃性物质的废液,置于燃烧炉中燃烧。如果数量很少,可把它装入铁制或瓷制容器,选择室外安全的地方把它燃烧。点火时,取一长棒,在其一端扎上沾有油类的破布,或用木片等东西,站在上风方向进行点火燃烧。并且,必须监视至烧完为止。
②对难于燃烧的物质,可把它与可燃性物质混合燃烧,或者把它喷入配备有助燃器的焚烧炉中燃烧。对多氯联苯之类难于燃烧的物质,往往会排出一部份还未焚烧的物质,要加以注意。对含水的高浓度有机类废液,此法亦能进行焚烧。
③对由于燃烧而产生NO2、SO2或HCl之类有害气体的废液,必须用配备有洗涤器的焚烧炉燃烧。此时,必须用碱液洗涤燃烧废气,除去其中的有害气体。
④对固体物质,亦可将其溶解于可燃性溶剂中,然后使之燃烧。
2).溶剂萃取法
①对含水的低浓度废液,用与水不相混合的正己烷之类挥发性溶剂进行萃取,分离出溶剂层后,把它进行焚烧。再用吹入空气的方法,将水层中的溶剂吹出。
②对形成乳浊液之类的废液,不能用此法处理。要用焚烧法处理。
3).吸附法
用活性炭、硅藻土、矾土、层片状织物、聚丙烯、聚酯片、氨基甲酸乙酯泡沫塑料、稻草屑及锯末之类能良好吸附溶剂的物质,使其充分吸附后,与吸附剂一起焚烧。
4).氧化分解法(参照含重金属有机类废液的处理方法)
在含水的低浓度有机类废液中,对其易氧化分解的废液,用H2O2、KMnO4、NaOCl、H2SO4+HNO3、HNO3+HClO4、H2SO4+HClO4及废铬酸混合液等物质,将其氧化分解。然后,按上述无机类实验废液的处理方法加以处理。
5).水解法
对有机酸或无机酸的酯类,以及一部份有机磷化合物等容易发生水解的物质,可加入NaOH或Ca(OH)2,在室温或加热下进行水解。水解后,若废液无毒害时,把它中和、稀释后,即可排放。如果含有有害物质时,用吸附等适当的方法加以处理。
6).生物化学处理法
用活性污泥之类东西并吹入空气进行处理。例如,对含有乙醇、乙酸、动植物性油脂、蛋白质及淀粉等的稀溶液,可用此法进行处理。
1 含一般有机溶剂的废液
一般有机溶剂是指醇类、酯类、有机酸、酮及醚等由C、H、O元素构成的物质。
对此类物质的废液中的可燃性物质,用焚烧法处理。对难于燃烧的物质及可燃性物质的低浓度废液,则用溶剂萃取法、吸附法及氧化分解法处理。再者,废液中含有重金属时,要保管好焚烧残渣。但是,对其易被生物分解的物质(即通过微生物的作用而容易分解的物质),其稀溶液经用水稀释后,即可排放。
2 含石油、动植物性油脂的废液
此类废液包括:苯、已烷、二甲苯、甲苯、煤油、轻油、重油、润滑油、切削油、机器油、动植物性油脂及液体和固体脂肪酸等物质的废液。
对其可燃性物质,用焚烧法处理。对其难于燃烧的物质及低浓度的废液,则用溶剂萃取法或吸附法处理。对含机油之类的废液,含有重金属时,要保管好焚烧残渣。
3 含N、S及卤素类的有机废液
此类废液包含的物质:吡啶、喹啉、甲基吡啶、氨基酸、酰胺、二甲基甲酰胺、二硫化碳、硫醇、烷基硫、硫脲、硫酰胺、噻吩、二甲亚砜、氯仿、四氯化碳、氯乙烯类、氯苯类、酰卤化物和含N、S、卤素的染料、农药、颜料及其中间体等等。
对其可燃性物质,用焚烧法处理。但必须采取措施除去由燃烧而产生的有害气体(如SO2、HCl、NO2等)。对多氯联苯之类物质,因难以燃烧而有一部分直接被排出,要加以注意。
对难于燃烧的物质及低浓度的废液,用溶剂萃取法、吸附法及水解法进行处理。但对氨基酸等易被微生物分解的物质,经用水稀释后,即可排放。
4 含酚类物质的废液
此类废液包含的物质:苯酚、甲酚、萘酚等。
对其浓度大的可燃性物质,可用焚烧法处理。而浓度低的废液,则用吸附法、溶剂萃取法或氧化分解法处理。
5 含有酸、碱、氧化剂、还原剂及无机盐类的有机类废液
此类废液包括:含有硫酸、盐酸、硝酸等酸类和氢氧化钠、碳酸钠、氨等碱类,以及过氧化氢、过氧化物等氧化剂与硫化物、联氨等还原剂的有机类废液。
首先,按无机类废液的处理方法,把它分别加以中和。然后,若有机类物质浓度大时,用焚烧法处理(保管好残渣)。能分离出有机层和水层时,将有机层焚烧,对水层或其浓度低的废液,则用吸附法、溶剂萃取法或氧化分解法进行处理。但是,对其易被微生物分解的物质,用水稀释后,即可排放。
6 含有机磷的废液
此类废液包括:含磷酸、亚磷酸、硫代磷酸及膦酸酯类,磷化氢类以及磷系农药等物质的废液。
对其浓度高的废液进行焚烧处理(因含难于燃烧的物质多,故可与可燃性物质混合进行焚烧)。对浓度低的废液,经水解或溶剂萃取后,用吸附法进行处理。
7 含有天然及合成高分子化合物的废液
此类废液包括:含有聚乙烯、聚乙烯醇、聚苯乙烯、聚二醇等合成高分子化合物,以及蛋白质、木质素、纤维素、淀粉、橡胶等天然高分子化合物的废液。
对其含有可燃性物质的废液,用焚烧法处理。而对难以焚烧的物质及含水的低浓度废液,经浓缩后,将其焚烧。但对蛋白质、淀粉等易被微生物分解的物质,其稀溶液可不经处理即可排放。